
Enfatizou-se que os padrões de aprovação dos kits de autoteste da FDA são mais altos do que os de reguladores estrangeiros, exceto nos Estados Unidos.
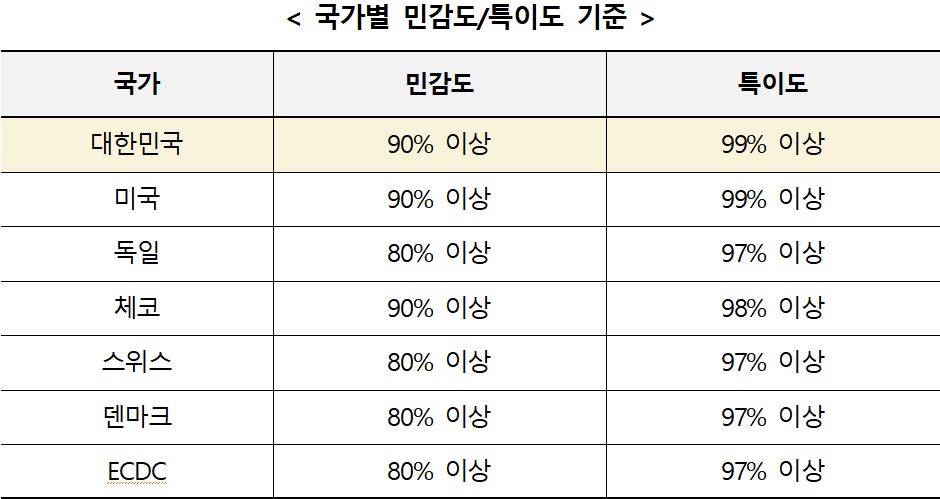
De acordo com o Departamento de Segurança de Alimentos e Medicamentos, o Departamento de Segurança de Alimentos e Medicamentos exige que os padrões de aprovação para os kits locais de autoteste COVID-19 tenham uma sensibilidade de 90% ou mais e uma especificidade de 99% ou mais. Por outro lado, órgãos reguladores em países estrangeiros como Alemanha e República Tcheca, com exceção dos Estados Unidos, que correspondem aos padrões coreanos, aplicam padrões mais baixos.
O Departamento de Segurança Alimentar e de Medicamentos explicou: “Foi aprovado fornecendo padrões de ensaios clínicos para demonstrar um nível de desempenho mais alto do que as agências reguladoras no exterior”.
Entre as medidas de desempenho dos grupos de autoteste, a sensibilidade refere-se à probabilidade de um paciente obter um resultado de teste positivo, e a especificidade refere-se à probabilidade de um resultado de teste ser negativo entre pacientes sem doença.
Enfatizou-se que a escala de ensaios clínicos do Padrão de Aprovação do Kit de Autoteste COVID-19 doméstico é equivalente ou requer mais participantes de ensaios clínicos do que os reguladores externos.
“Os kits de autoteste aprovados na Coreia são projetados para ter uma proporção de casos confirmados e não confirmados de aproximadamente 1:2 entre os sujeitos em ensaios clínicos”, disse o Ministério da Segurança Alimentar e de Medicamentos (MFDS).
Ele continuou: “No local de teste real, o teste é realizado em pessoas que não sabem se estão infectadas ou não, e o valor preditivo positivo (a porcentagem de infecção verdadeira confirmada por PCR entre grupos de autoteste positivo) pode variar dependendo do estado de infecção que difere dos ensaios.” Clínico.
Alguns kits de autoteste aprovados na Coréia por seu desempenho foram reconhecidos na comunidade internacional, como a aprovação para uso emergencial por agências reguladoras estrangeiras, como Estados Unidos e Canadá.
De acordo com o Departamento de Segurança de Alimentos e Medicamentos, os produtos SD Biosensor e Humasys estão atualmente aprovados para uso a longo prazo nos Estados Unidos, e os produtos Sugentech são usados no Canadá.
Enquanto isso, o Departamento de Segurança de Alimentos e Medicamentos disse: “Para melhorar a precisão do kit de autoteste, é importante ler atentamente o manual de instruções anexado ao produto e usar o kit corretamente”. Encontrado no blog do Ministério de Segurança de Alimentos e Medicamentos (blog.naver.com/kfdazzang/222640236513). “

“Leitor implacável. Especialista em mídia social. Amante de cerveja. Fanático por comida. Defensor de zumbis. Aficionado por bacon. Praticante da web.”
